炎症性肠病IBD研究模型:溃疡性结肠炎首 个靶向IL-23p19生物制剂获批
10月27日,礼来宣布FDA已批准mvoh (mirikizumab)上市,用于治疗中重度活动性溃疡性结肠炎(ulcerative colitis,UC) 成人患者,这是首 个用于治疗这一患者群体的IL-23p19拮抗剂。Mirikizumab是一种人源化lgG4单克隆抗体,能够特异性地与IL-23的p19亚基结合,从而阻断IL-23介导的炎症反应。
炎症性肠病IBD,你知道多少?
炎症性肠病(inflammatory bowel disease, IBD)是病因不明的非特异性肠道炎症,其中最主要的两种类型是UC和克罗恩病(Crohn disease, CD),主要区别在于CD可累及消化道的任何部位,而UC几乎仅累及结肠。两种疾病导致的长期腹泻可能使患者体重减轻并出现营养不良。有时,炎症性肠病可影响身体其他部位,如关节、眼睛、口腔、肝脏、胆囊和皮肤,也可能增加肠道受累部位癌变的风险。
IBD是由遗传和环境诱因使患者消化道微生物组分发生变化,肠道屏障完整性被破坏,同时患者伴有免疫系统失调,肠黏膜中的效应细胞和调节细胞之间失衡,错误攻击自身健康细胞,从而导致持续的炎症。IBD影响全球约600-800万人,治疗手段有限且仍有提升空间,现有疗法仅有10%-15%的患者病情缓解,严重情形下患者可能会被切除结肠。
据统计,2021年美国IBD药物市场约为150亿美元,并仍在高速增长,其中Entyvio、Humira和Stelara在IBD适应症上的总销售规模已达到120亿美元。2023年4月,默沙东以总交易额108亿美元收购Prometheus Biosciences获得其核心管线,一款治疗IBD的TL1A抗体PRA023;2023年6月,礼来以24亿美元的价格收购DICE Therapeutics,囊获包括治疗银屑病的IL-17小分子抑制剂、治疗IBD的α4β7单抗在内的多款自免药物;2023年10月,罗氏宣布将以70亿美元的价格收购Roivant Sciences的TL1A抗体RVT-3101。几笔大交易不断加码IBD赛道热度,而火热的背后,反映的是IBD高度未满足的临床需求。
IBD治疗药物发展史
IBD的传统治疗药物包括糖皮质激素、抗生素、免疫抑制剂、氨基水杨酸等。随着靶向TNF-α的英夫利西单抗和阿达木单抗获批UC/CD适应症后,IBD也宣告进入了“生物制剂”时代。在此之后,IL-12抗体乌司奴单抗、α4β7抗体维得利珠单抗、JAK抑制剂乌帕替尼等药物的相继获批,填补了传统治疗或TNF-α抗体药物应答不足或无法耐受的IBD患者的治疗空白。80%的IBD患者会慢性复发,20%~30%患者在多次复发后不得不进行手术治疗,切除部分肠道,这严重影响了患者的生活质量。因此,目前IBD患者仍有着巨大的未满足临床需求,迫切需要开发有效的治疗方法来解决这一全球健康问题。
集萃药康炎症性肠病IBD小鼠模型资源
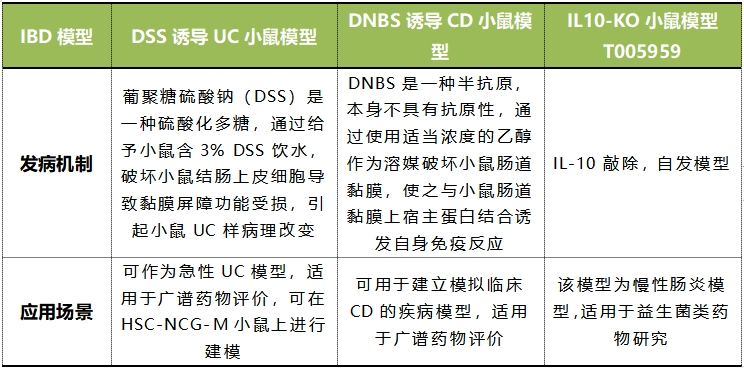
集萃药康自免平台可提供小鼠模型和相关技术服务,针对IBD,集萃药康开发了多款炎症性肠病IBD小鼠模型可用于临床前药效评价。
部分炎症性肠病IBD模型数据展示
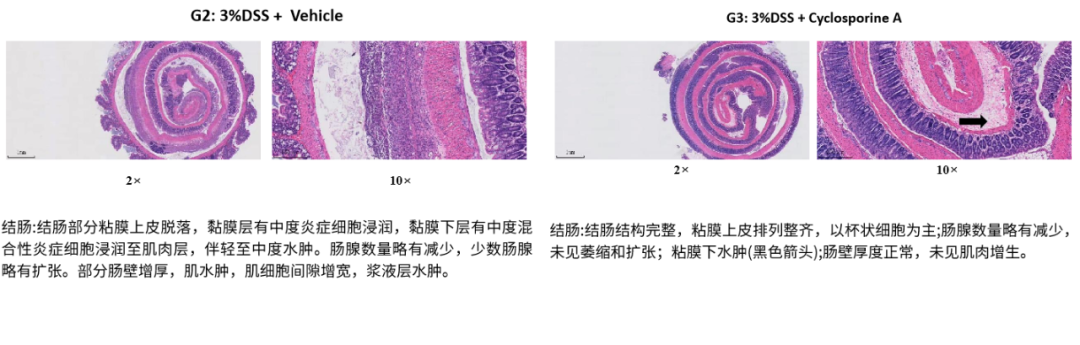
环孢霉素A可改善DSS诱导的UC模型的疾病表型
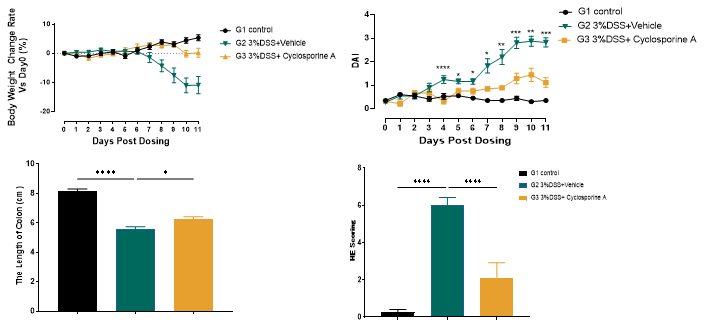
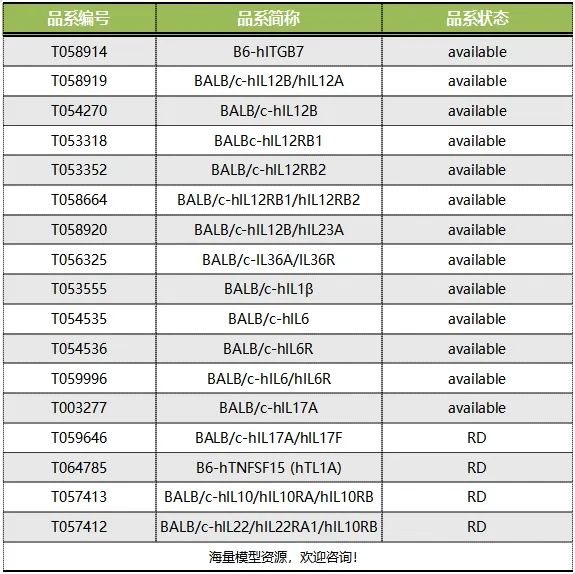
炎症性肠病IBD相关靶点人源化小鼠资源