万众瞩目!集萃药康FCGR全人源化小鼠上市了!
在医学研究中,人源化小鼠模型能够更加真实地模拟人类的生物学特性,使得疾病机制的研究、药物筛选和临床前实验更加接近真实人体环境,极大地提高研究的可靠性和转化效率。近日,集萃药康自主研发的FCGR全人源化小鼠模型——BALB/c-hFcgRs正式上市,为国内抗体药物的研发事业提供了有力支持。
FCGR全人源化小鼠模型的诞生
随着越来越多的抗体类药物获批上市,抗体药物在肿瘤、自身免疫性疾病、代谢疾病等治疗领域的研究均取得了令人欣喜的进展。抗体的结构分为两部分:Fab端和Fc端。Fab端负责识别肿瘤细胞或肿瘤微环境(TME)中非肿瘤细胞中的游离分子或细胞表面受体;Fc端负责与效应细胞结合引发细胞杀伤作用,包括抗体依赖的细胞介导的细胞毒性作用(ADCC)、抗体依赖性细胞介导的吞噬作用(ADCP)以及补体依赖的细胞毒性作用(CDC)。不同抗体的Fc端重链不同,对应的受体也不同,人类IgG抗体的受体包括FCGRIA/IB (CD64A/B)、FCGRIIA/IIB/IIC (CD32A/B/C)、FCGRIIIA/IIIB (CD16A/B)。其中,FCGRIIB是小鼠和人类FCGR中唯一一个抑制性受体,抗体Fc端与这些受体结合会引发不同的生物学效应[1]。
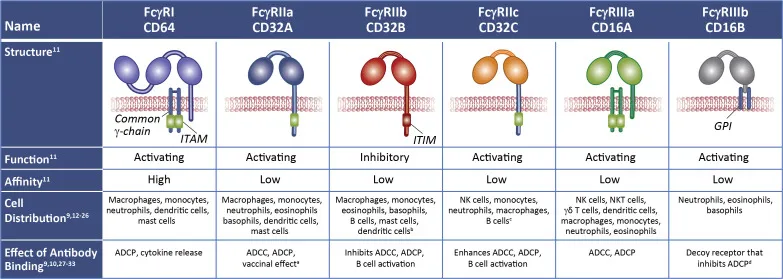
图1.人体中不同FCGR的表达及功能
ADCC,作为抗体药物发挥药效的重要机制之一,主要通过NK细胞表面的FCGRIIIa受体与Fab端结合了肿瘤细胞的抗体Fc端结合形成免疫突触,触发穿孔素和颗粒酶的分泌,从而诱导肿瘤细胞死亡[1]。由于小鼠和人的IgG受体类型和表达分布存在很大差异(图2),无法使用普通的小鼠评价人源抗体的体内药效,为了解决这一难题,江苏集萃药康自主研发了FCGR全人源化的小鼠模型——BALB/c-hFcgRs,助力国内抗体药物的研发事业。
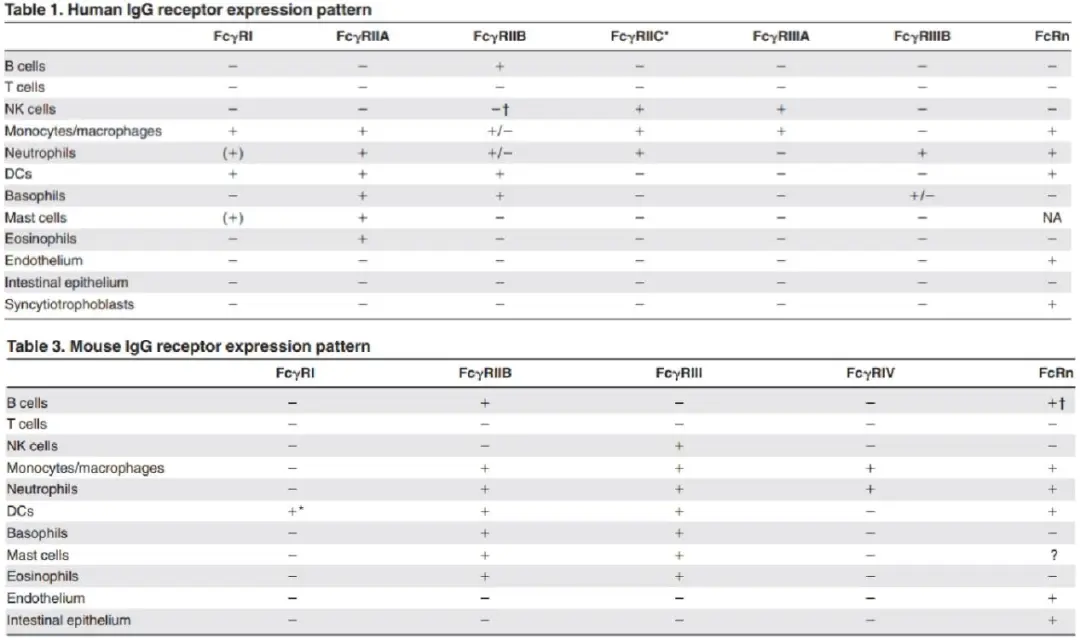
图2.人源和鼠源FCGR类型及表达分布[2]
FCGR全人源化小鼠模型的构建和验证
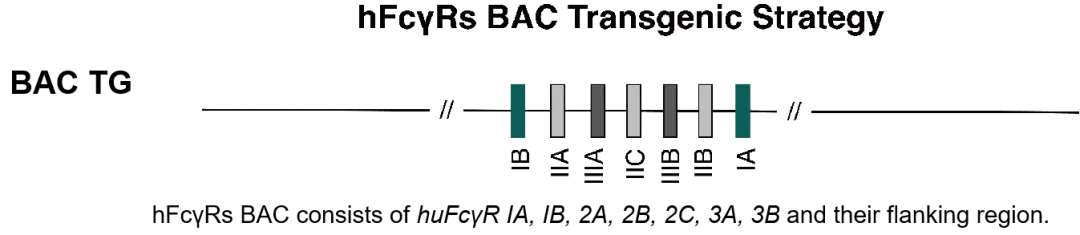
图3. hFcγRs BAC结构示意图
集萃药康采集BALB/c小鼠或BALB/c-hFcgRs(hFcgRs-TG/mFcgRs-KO)外周血,使用商品化的相应抗体,检测了人源FCGR在各个免疫细胞上的表达情况,其中,NK细胞上的hFCGR3A表达80%左右,具体见下图。
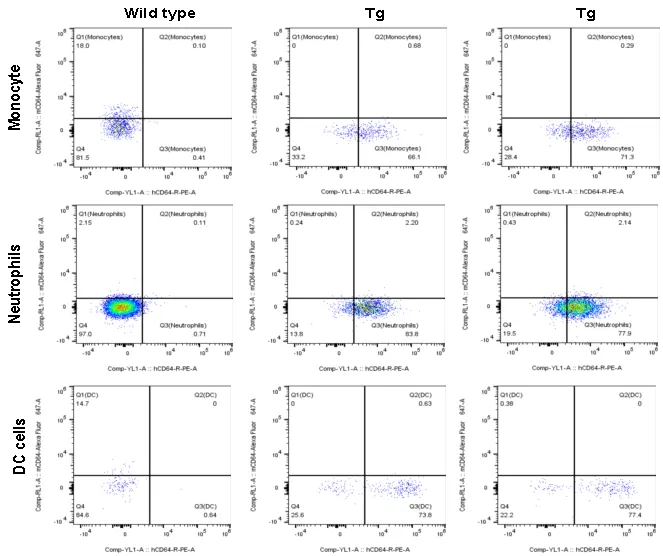
图4.单核细胞、中性粒细胞及树突细胞表面的hFCGR1(hCD64)表达检测
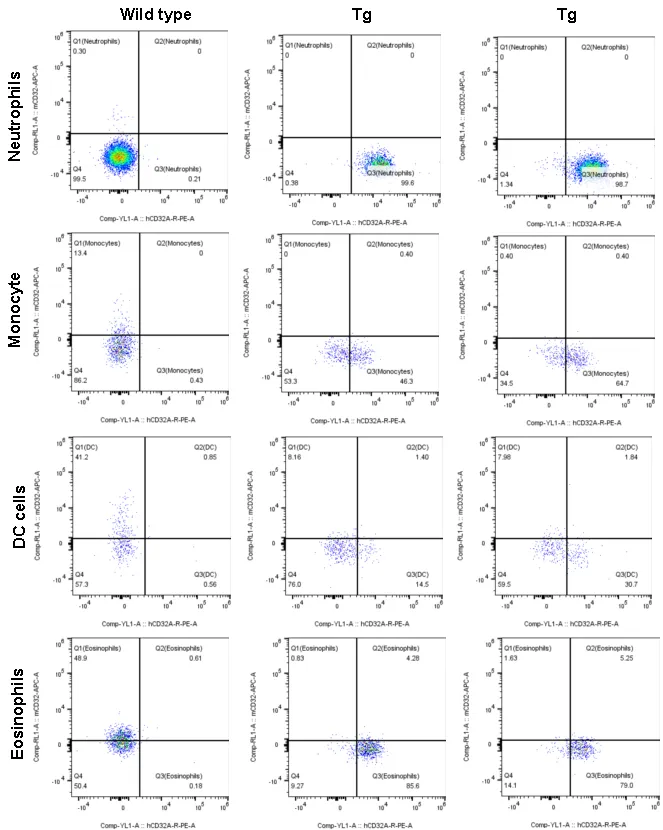
图5.中性粒细胞、单核细胞、树突细胞、嗜酸性粒细胞表面的hFCGR2A(hCD32A)表达检测
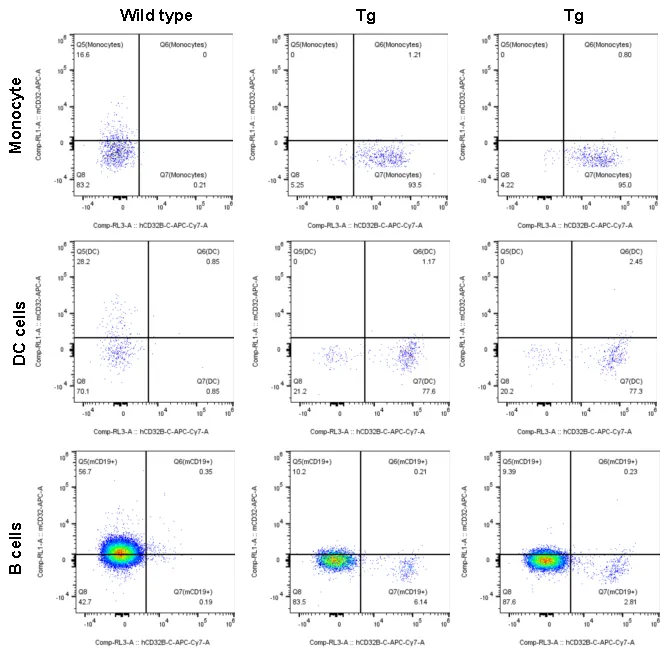
图6.单核细胞、树突细胞及B细胞表面的hFCGR2B/C(hCD32B/C)表达检测
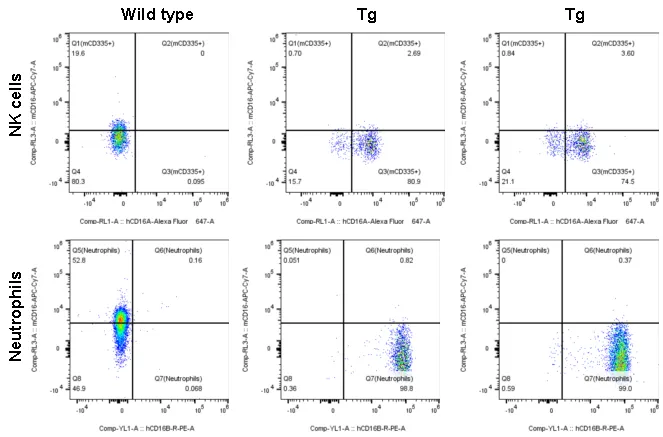
图7.NK细胞表面hFCGR3A(hCD16A)和中粒细胞hFCGR3B(hCD16B)表达检测
动物模型在现代生物医学研究中扮演着不可或缺的角色,广泛应用于疾病生理病理的基础科学研究、转化医学研究以及新治疗方法的探索过程中。除了FCGR全人源化小鼠模型,集萃药康还提供各类高质量人源化小鼠模型,在基因、免疫系统、特定细胞、组织以及微生物群落中表达与人类相似的生物特征。欢迎咨询深入了解。
参考文献
1.Musolino A, et al. J Immunother Cancer 2022;10:e003171.
2.Bruhns P, et al. Blood. 2012;119(24):5640-5649.

