
B6-hPCSK9人源化模型及其药效评价
随着生活水平的提高,人们饮食结构的改变,高脂血症( hyperlipidemia,HLP) 发病率越来越高,HLP 严重危害着人类的身体健康,因为长期血脂过高会引发机体代谢紊乱,进而产生动脉粥样硬化、冠心病、心肌梗死等心脑血管疾病。因此,对高脂血症的预防和相关治疗药物开发尤为重要。
PCSK9是一种已知的分泌因子,可负向调节细胞膜上LDLR的表达水平。PCSK9主要在肝组织中表达。分泌的PCSK9与LDLR结合,在溶酶体的作用下降解。对人类PCSK9基因的研究表明,PCSK9功能获得性突变与家族性高脂血症有关,PCSK9功能丧失性突变的LDL-C水平比普通人低15%~28%。因此,PCSK9是胆固醇代谢途径中的重要调节因子。抑制PCSK9表达水平或活性可以显着降低“坏”LDL-C 的水平。因此,PCSK9是开发抗高脂血症药物的有效靶点。
品系:B6/JGpt-Pcsk9em1Cin(hPCSK9)/Gpt
动物使用量:8~10只/组,3~5组
实验阶段:8~10 周
1. 研究概览
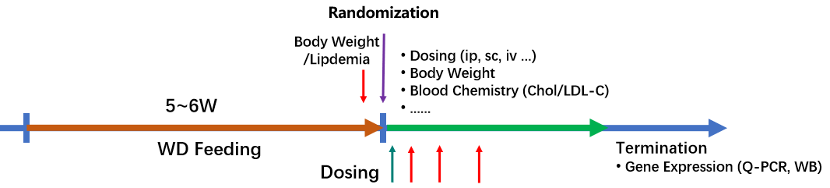
图1. B6-hPCSK9小鼠研究概览。B6-hPCSK9小鼠可通过喂食高胆固醇饮食而发生高脂血症。
2. hPCSK9人源化模型验证数据
(1)hPCSK9 mRNA与mPCSK9 mRNA检测

图2. 在B6-hPCSK9小鼠(5周龄)的肝脏中,只有人源PCSK9 mRNA表达,而小鼠PCSK9 mRNA不表达。数据以Mean±SD展示,n=8。
(2)hPCSK9蛋白水平检测

图3. 在B6-hPCSK9小鼠的肝脏中检测到hPCSK9蛋白,而在C57BL/6J小鼠(5周龄)的肝脏中未检测到.
(3)LDLR蛋白水平检测
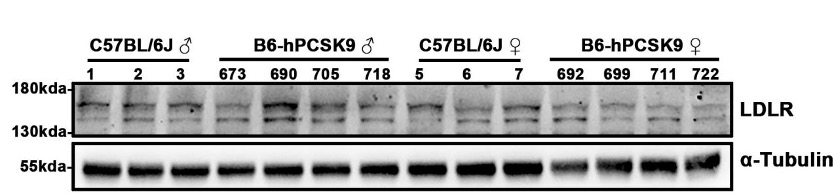
图4. C57BL/6J与B6-hPCSK9小鼠(5周龄)肝脏中LDLR表达无明显差异。
(4)LDL-C水平检测

图5. C57BL/6J与B6-hPCSK9小鼠(8周龄)血浆LDL-C水平无显著性差异.
3. hPCSK9人源化模型药效测试数据
(1)药物(evolocumab)干预饮食诱导的hPCSK9人源化小鼠后血脂水平下降
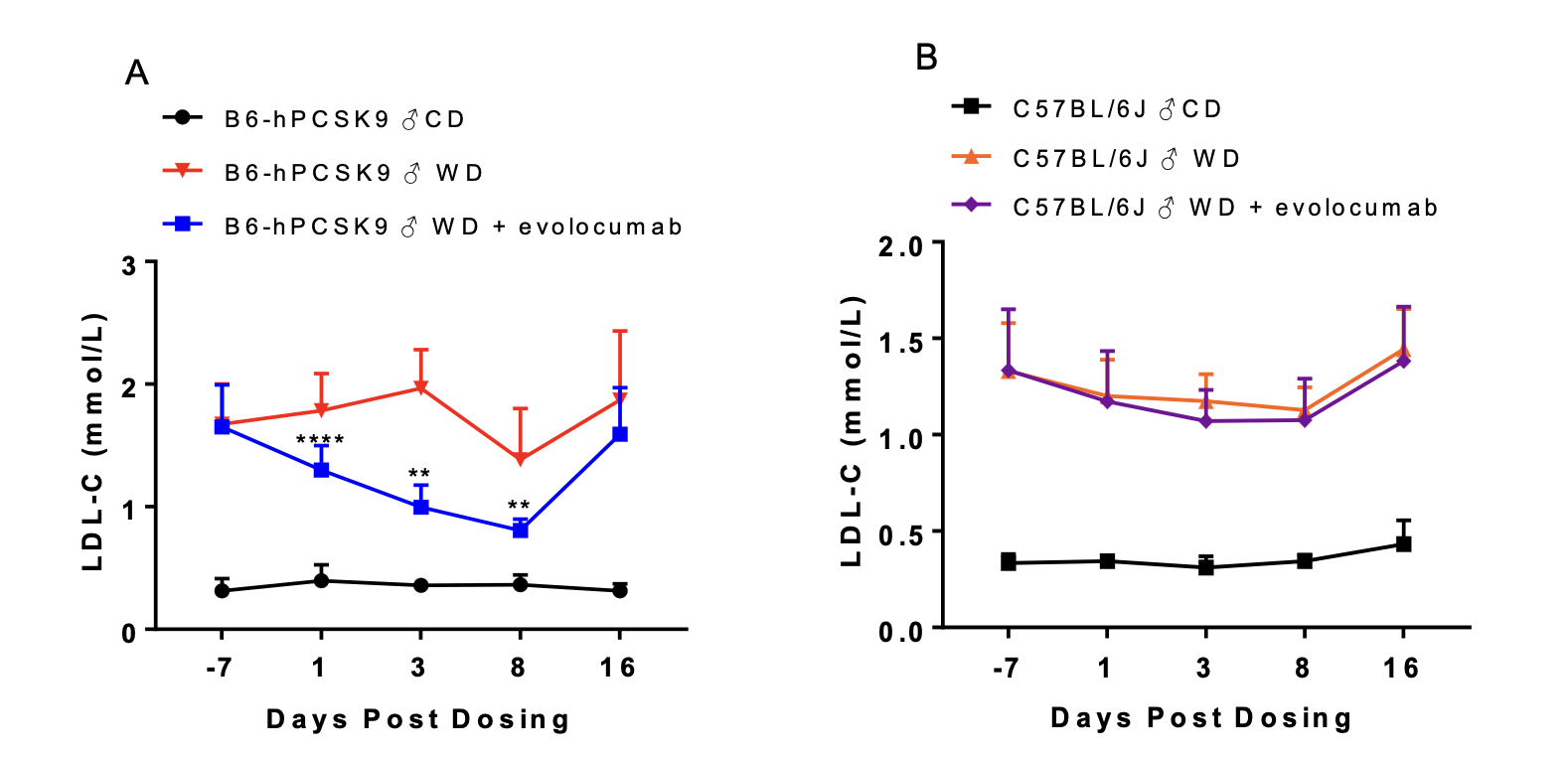
图6. 单次尾静脉注射exvolocumab(20mpk)可以显著降低西方饮食喂养的B6-hPCSK9小鼠血浆LDL-C水平,但在西方饮食喂养的C57BL/6J小鼠中没有观察到类似的效果。
使用unpaired two-tailed Student's t-test方法进行统计学分析。**,p<0.01;***,p<0.001 与对照B6-hPCSK9+WD相比。
(2)exvolocumab显著增加饮食诱导的hPCSK9人源化小鼠LDLR水平
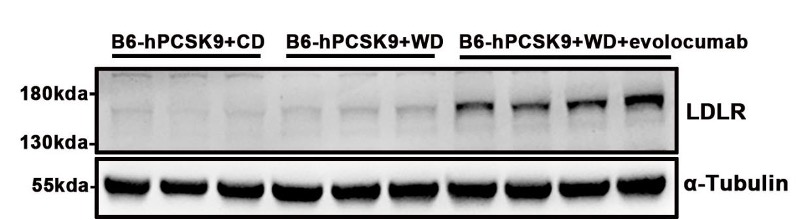
图7. 单次尾静脉注射 evolocumab 单抗(20mpk)后3天,西方饮食喂养的B6-hPCSK9小鼠肝脏LDLR的表达水平显著升高。
(3)测试药物验证数据

图8. 测试药物X(siRNA靶向hPCSK9)显著降低了WD喂养的B6-hPCSK9小鼠的血浆LDL-C水平。数据以Mean±SD展示,n=5。
使用unpaired two-tailed Student's t-test方法进行统计学分析。**,P<0.01;***,P<0.001。

