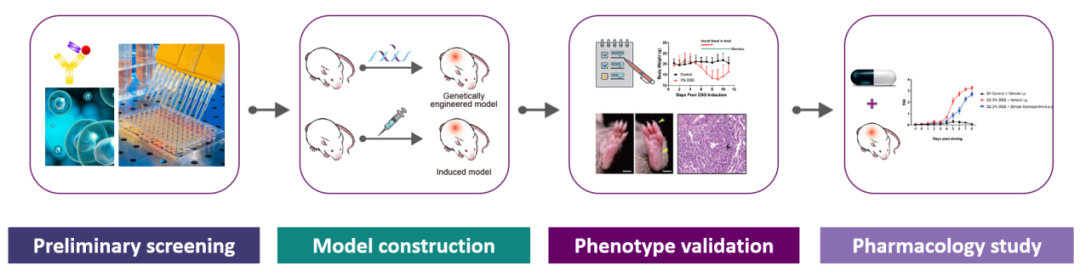
STING通路再下一城!靶向RNF115改善STING依赖性炎症和自身免疫的研究
2024年,武汉大学林丹丹、钟波及陈小奇共同通讯在国际著名期刊cellular & molecular immunology(CMI)上发表了名为“Disulfiram ameliorates STING/MITA-dependent inflammation and autoimmunity by targeting RNF115”的研究论文。STING是cGAS下游的一种细胞质DNA感应蛋白,可介导细胞质DNA 触发的信号转导,通过胞质自身DNA或功能获得突变对STING的异常激活引起严重炎症。研究团队发现RNF115能促进STING介导的炎症和自身免疫,而RNF115抑制剂双硫仑(DSF)能改善炎症和自身免疫,在Trex1 KO小鼠和STINGN153S/WT骨髓嵌合小鼠中发现,敲除RNF115或用DSF治疗可显著抑制全身炎症和自身免疫致死性,恢复免疫细胞发育。该研究使用了来自集萃药康自主产权的Trex1 KO小鼠(Strain NO. T013987)及Rnf115–/– 小鼠(Strain NO. T044759),以及集萃药康提供的STINGN153S/WT 小鼠。

Trex1是一种降解自身DNA的DNA外切酶,Trex1的功能丧失突变与人类自身免疫性疾病密切相关,如Aicardi-Goutieres综合征(AGS)、视网膜血管病变伴脑白质营养不良(RVCL)以及系统性红斑狼疮(SLE)。在稳态条件下,宿主DNA被隔离在细胞核或线粒体中。但是当Trex1敲除后,会导致细胞质中自身DNA的累积和cGAS-cGAMP-STING通路的持续激活,从而引发自身免疫反应。因此,Trex1 KO小鼠会出现严重的全身炎症,并表现出严重的自身免疫反应,这种现象会通过RNF115的缺失在基因上得到改善,这表明STING在自身DNA引起的自免疾病中发挥着至关重要的作用。
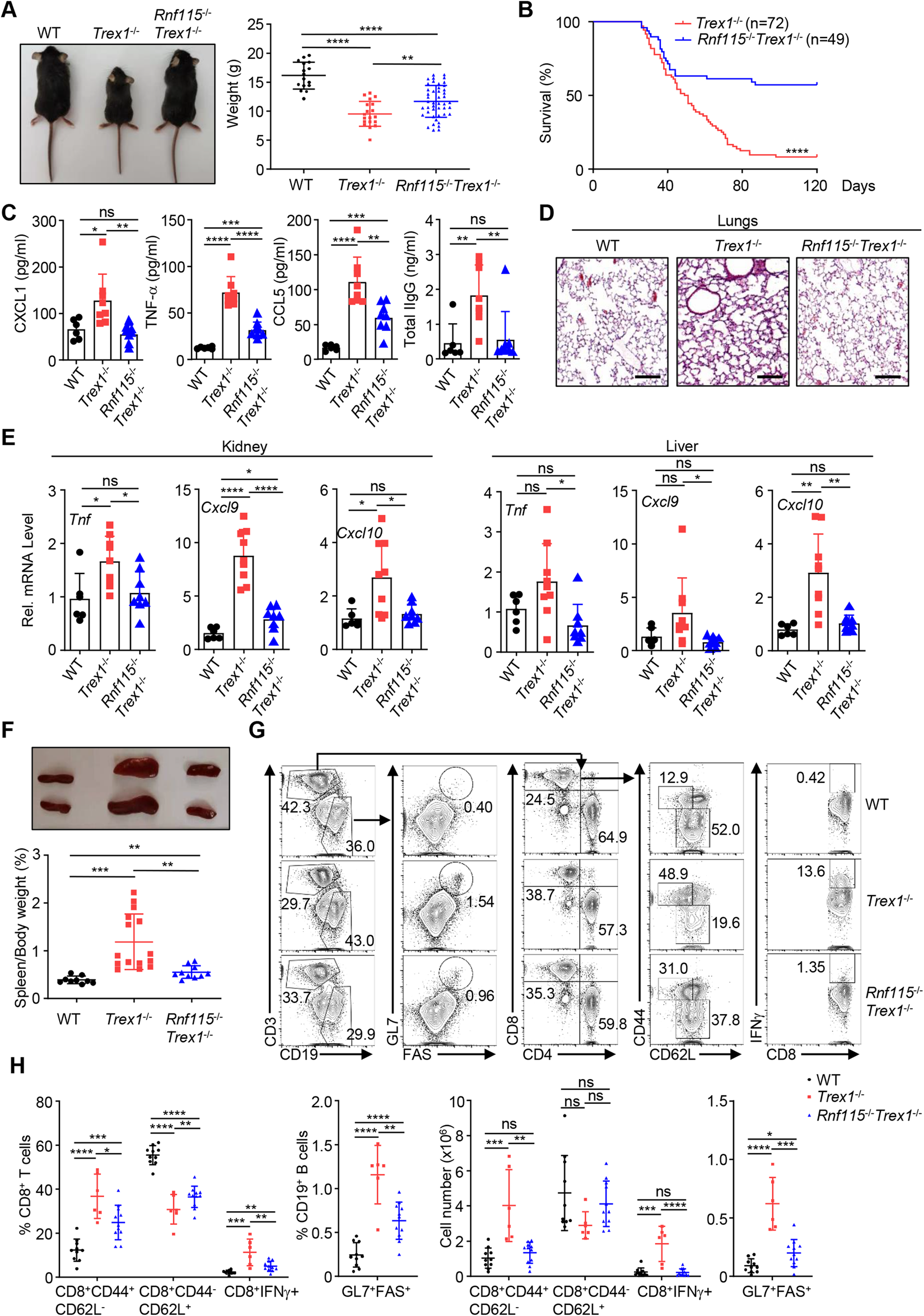
图1:Deletion of RNF115 attenuates the autoimmune phenotypes of Trex1–/– mice.
除了胞质DNA外,STING的功能突变(其中最常见的是STINGN154s和STINGV155M)介导下游信号通路的激活,导致了STING的自身免疫性疾病,与婴儿期发病相关的血管病变(SAVI)。研究STING通路激活的具体调控机制和靶向激活的STING通路将为自身免疫病相关药物的开发提供治疗策略。
该研究报道RNF115是一种E3连接酶,在Trex1 KO细胞和组织中与STING相互作用。RNF115可以通过催化STING或STINGN153S来促进STING通路介导的炎症和自身免疫性反应,使用RNF115抑制剂双硫醚(DSF)可以减弱STING介导的相关免疫反应。同时,RNF115的缺失或药理抑制可减弱Trex1 KO小鼠和STINGN153S/WT骨髓嵌合小鼠的自身免疫表型。SLE是一种多系统自身免疫性疾病,以自身抗体产生和多器官损伤为特征。SLE病人血清中dsDNA含量显著升高,病人PBMC中STING活性明显升高。研究团队通过收集SLE病人血液分离血清和PBMC,发现敲除RNF115及DSF治疗能够显著抑制SLE病人的PBMC中炎症因子和干扰素的表达,该研究结果强调了STING受RNF115调控作为自身免疫性疾病治疗干预靶点的过程。
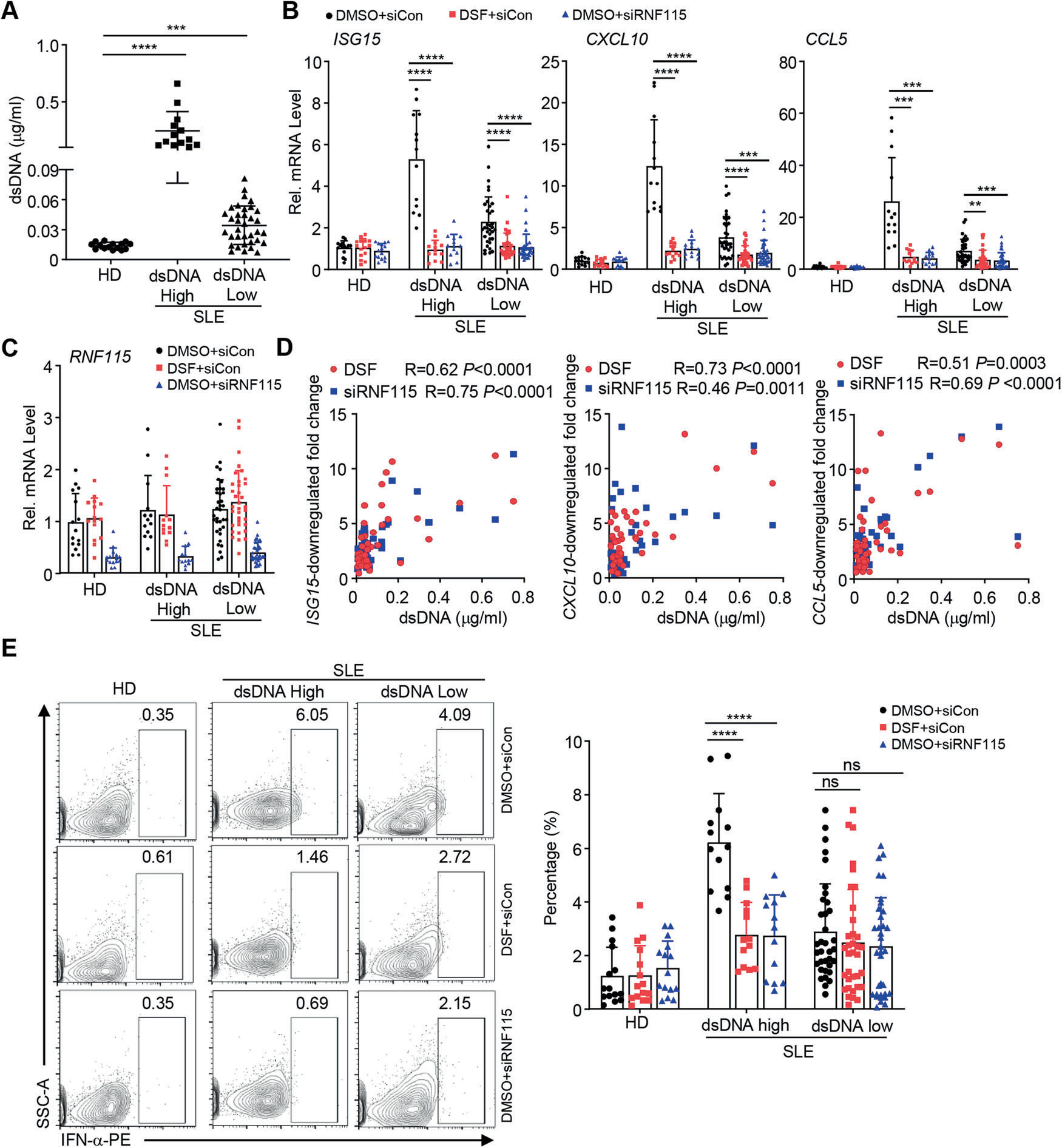
图2:Inhibition of RNF115 downregulates the expression of proinflammatory cytokines in PBMCs from SLE patients.
这项研究说明了在炎症状态下靶向RNF115可显著改善STING相关的炎症表型,预示DSF可能会成为治疗STING相关疾病的潜在治疗药物。未来,集萃药康会更加关注STING通路引起的自身免疫性反应,为药物研发筑路。
以上数据引用均获得第 一作者许可。
集萃药康自免平台主要聚焦系统性红斑狼疮、炎性肠病、多发性硬化症、银屑病、特应性皮炎、类风湿性关节炎、免疫性肾病等多种疾病领域,可提供动物模型和技术服务,并可定制药物开发非临床一站式服务。